
임정훈 교수팀이 기념사진을 촬영하고 있는 모습. 맨 뒷줄 하얀색 가운을 입은 사람이 임정훈 교수. [사진=UNIST(울산과기원)]
아주경제 울산 정하균 기자 = UNIST(울산과학기술원)는 임정훈 생명과학부 교수팀이 퇴행성 뇌질환 유전자인 '어택신-투'(Ataxin-2)와 결합하는 새로운 생체시계 유전자를 발견, 생체리듬을 조절하는 분자생물학적 원리를 세계 최초로 규명했다고 7일 밝혔다.
생화학 및 분자생물학 분야 최고 권위의 학술지 '몰레큘러 셀'(Molecular Cell) 6일자에 발표된 이 논문은 루게릭병의 발병 원인과 치료 연구에도 중요한 단서가 될 전망이다.
어택신-투 유전자의 돌연변이는 루게릭병, 척수소뇌실조증, 파킨슨병 등과 같은 퇴행성 뇌질환의 중요한 유전적 요인으로 작용한다. 하지만 노화에 따른 신경세포 사멸과 퇴행성 뇌질환 발병을 조절하는 '어택신-투 단백질 복합체’의 분자생물학적 작용 원리에 대해서는 지금껏 알려지지 않았다.
임 교수는 2011년 네이처(Nature)와 2013년 사이언스(Science)에 발표한 연구를 통해 생체시계 유전자인 피어리어드(period) 단백질 합성에 필요한 새로운 유전자 트웬티-포(twenty-four)를 발견했다.
어택신-투가 트웬티-포 단백질의 번역 활성화 기능을 촉진함으로써 수면 주기와 같은 24시간 주기의 일주기성 동물 행동을 조절한다는 생체시계의 작동원리를 규명한 것이다. 피어리어드는 최초로 밝혀진 생체시계 유전자로 이 유전자를 조작하면 생체리듬에 이상이 생긴다.
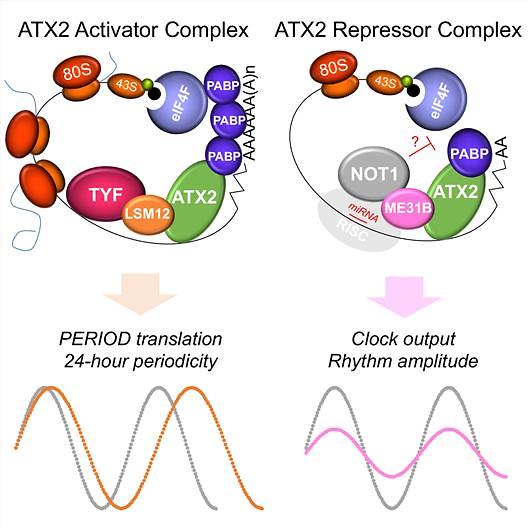
어택신-투 결합 단백질에 따른 단백질 복합체의 기능 변화 모형도.
이번 연구에선 어택신-투 단백질과 결합하는 두 개의 새로운 단백질에 대한 유전자(Lsm12, me31B)를 발견하고, 각 단백질의 결합에 따라 달라지는 어택신-투 단백질 복합체의 생체리듬 조절 원리를 밝혀냈다. 이러한 분자생물학적 작용 원리 규명엔 형질전환 초파리의 행동신경 유전학적 모델이 활용됐다.
새로 발견된 '엘에스엠-트웰브' 단백질은 어택신-투와 트웬티-포 단백질을 연결시키는 분자 어댑터로 작용한다. 그 결과 생체시계 유전자인 피어리어드 단백질 번역을 활성화시키고, 생체리듬이 24시간의 주기성을 가지도록 만든다.
반면 엠이써티원비 단백질은 어택신-투 단백질과 결합해 단백질 번역의 재료인 전령 RNA를 분해하는 낫원(Not1) 단백질 기능을 활성화시킨다. 그 결과 생체리듬을 조절하는 물질(신경 펩타이드)의 분비 시기를 조절해 수면 등 생체리듬의 주기를 지속시키는 역할을 한다고 연구팀은 설명했다.
임정훈 교수는 "이번 연구는 루게릭병과 같은 퇴행성 뇌질환 발병 원인을 이해하는 근본적인 분자생물학적 모델을 확립했다는 데 의미가 있다"며 "이런 결과를 토대로 어택신-투 단백질 복합체가 어떤 세포생물학적 경로를 통해 루게릭병의 발생에 기여하는지 구체적으로 연구하고 있다"고 전했다.
이번 연구는 UNIST 생명과학부 석·박사통합과정 이종보·유은석·이호연 연구원이 공동 제1저자로 참여했다. 연구 지원은 미래창조과학부·한국연구재단의 신진연구지원사업과 보건복지부·한국보건산업진흥원의 질환극복기술개발사업(질병중심 중개기반연구)을 통해 이뤄졌다.
©'5개국어 글로벌 경제신문' 아주경제. 무단전재·재배포 금지


![[르포] 중력 6배에 짓눌려 기절 직전…전투기 조종사 비행환경 적응훈련(영상)](https://image.ajunews.com/content/image/2024/02/29/20240229181518601151_258_161.jpg)



